중소병원 의료기관 종사자의 COVID-19 AstraZeneca (ChAdOx1) 백신 접종 영향요인과 접종 후 이상 반응 실태조사
Factors Influencing COVID-19 AstraZeneca (ChAdOx1) Vaccination and Side Effects among Health Care Workers in an Acute General Hospital
Article information
Abstract
Purpose: This study was conducted to identify factors affecting COVID-19 vaccination and associated side effects among health care workers in a small and medium-sized hospital. Methods: In May 2021, 301 workers out of a total of 670 working in a small and medium-sized hospital in Gyeonggi-do, were surveyed. The small and medium-sized hospital treats patients with COVID-19. Health care workers across different medical institutions responded with self-reported internet questionnaires. Factors influencing COVID-19 vaccination were analyzed via logistic regression. Results: Out of 301 subjects, 89.0% showed an intention to inoculate, and 85.7% were vaccinated against COVID-19. The most frequent reason for vaccination was responsibility as a medical worker. The fear of adverse reactions was the most frequent reason for non-vaccination. Adverse reactions after inoculation occurred in 70.9% of cases, and 30.6% were referred for treatment of adverse reactions. The factors ultimately influencing COVID-19 vaccination were vaccination intention, previous side effects from other vaccinations, occupation, and age. Conclusion: In order to improve the effectiveness of COVID-19 vaccination, a systematic approach is required to determine the risk factors associated with the young age of the administrative staff/personnel, subjects with a history of side effects associated with other vaccines, and health care workers who do not intend to be vaccinated. It is important to develop strategies to improve immunization. In addition, accurate and essential information regarding the side effects of vaccination is needed, along with appropriate education and publicity.
서 론
1. 연구의 필요성
2019년부터 시작된 COVID-19의 세계적대유행은 광범위한 이환율과 사망률을 야기하고 있다. 범유행(汎流行) 또는 세계적 대유행(世界的大流行)은 전염병이나 감염병이 범지구적으로 유행하는 것이다. 영어로 팬데믹(pandemic)으로 부르기도 한다. World Health Organization (WHO)는 1968년 홍콩독감과 2009년 신종 인플루엔자 A (H1N1)에 팬데믹 선언을 하였다. 이후 2020년 3월 11일 최고 단계인 팬데믹6단계를 선언하였다[1,2]. 이전에도 스페인독감 (Severe Acute Respiratory Syndrom, SARS), 인플루엔자 등의 유행상황은 존재하였으며 이를 극복하기 위한 인간의 노력은 끊임없이 이어졌다. 1918년 스페인독감 대유행은 20세기에 인류가 직면한 최초의 치명적인 팬데믹 상황이었다. 1918년 스페인 독감유행이후 100년이 지난 지금 또 다른 치명적인 대유행 상황에 직면해 있다[2]. 각 국가에서는 COVID-19 극복을 위해 전력을 다하고 있다[1,3]. COVID-19 치료제 개발과 백신개발을 위한 노력은 역사상 유례가 없었던 상황이다. 2009년 인플루엔자 유행 시에는 이미 인플루엔자 치료제가 개발되어 있었고, 계절성 인플루엔자 백신 접종이 해마다 시행되고 있었다는 부분이 COVID-19 상황과는 다르다[4]. COVID-19 치료제와 백신 개발에 대한 노력의 결과로 여러 백신이 3상 효능의 목표에 도달하였고, 2020년 말까지 긴급사용 승인이 이루어졌다[5,6].
2021년 2월까지 COVID-19 백신접종은 Pfizer의 BNT162b2와 Moderna의 mRNA-1273, Janssen의 JNJ-78436735 (Ad26.COV2.S), AstraZeneca의 AZD1222 (ChAdOx1), 중국의 CoronaVac, 러시아의 SPUTNIK 등이 개발되었다. Pfizer와 Moderna는 mRNA백신이며, ChAdOx1 nCoV-19 백신(AZD1222)은 SARS-CoV-2 스파이크 삽입이 포함된 침팬지 아데노바이러스 벡터 백신이다[6,7].
국내 첫 COVID-19 접종백신은 Pfizer의 BNT162b2와 AstraZeneca의 AZD1222 (ChAdOx1)로 2021년 2월 26일부터 시작하였다. 접종대상은 65세 이상을 제외한 요양기관 입소자와 의료기관 종사자 등 크게 4분류로 나누어 우선순위에 따라 시행되었다. 특히 COVID-19 관련 업무에 관여하는 의료기관종사자의 접종은 2021년 3월4일부터 시작되었는데 코로나 관련 업무에 종사하거나 환자치료에 참여가능성이 있는 의료진이 우선순위로 선정되었다[7].
영국연방의 조사에 의하면 COVID-19 AstraZeneca (ChAdOx1) 백신은 접종 후 주사 부위 압통 및 통증, 두통, 피로, 근육통, 불쾌감, 38°C 미만 발열, 38°C 이상 발열, 오한, 관절통 및 메스꺼움 등의 증상이 보고되었다[8]. 대부분의 이상 반응은 경증에서 중등도였으며, 일반적으로 예방 접종 후 며칠 내에 호전되었다. 접종 후 일주일 이상 적어도 하나 이상의 국소 또는 전신 반응을 보이는 접종자의 이상반응 발생률은 약 4%-13%로 보고되었다. AstraZeneca (ChAdOx1)백신의 2차 접종의 부작용보고는 1차 접종에 비해 이상반응이 가볍고 빈도가 줄었다고 보고하고 있다[8].
2021년 4월에 보고된 국내에서 의료기관 종사자 994명을 대상으로 COVID-19 백신접종 후 이상반응에 대한 보고가 이루어졌다. 전신증상으로 피로 92.9%와 불쾌감 83.8%이었고 38°C 이상의 발열이 27.6%였다. 소수에서 40°C 이상의 발열과 설사 등이 보고되었다[9]. 또한 Bae 등[10]은 COVID-19 백신 접종자 5,866명을 대상으로 Pfizer의 BNT162b2와 AstraZeneca의 AZD1222 (ChAdOx1) 접종 후 이상반응을 비교하였다. Pfizer의 BNT162b2를 접종한 경우보다 AstraZeneca의 AZD1222 (ChAdOx1)를 접종한 경우 이상반응을 완화하기 위한 약물투여가 9.5배 더 높았다.
백신접종이란 면역형성을 위한 수단 중 하나이지만 이에 따른 부작용도 불가피한 것이 사실이다. 일반적으로 백신접종 후 접종부위의 발적과 통증, 발열, 무력감, 두통의 전신 반응이 보고되나 1-2일내에 사라진다. 드물게는 아낙필락시스와 같은 과민반응이나 길랑-바레증후군과 같은 중증의 이상반응도 보일 수 있다[11]. 2009년 신종 인플루엔자 A (H1N1) 팬데믹 당시 백신인 Pandemrix의 접종 후 기면증 발생으로 인해 백신의 안전성에 대한 문제가 제기되었다. 이는 백신에 대한 불신으로 이어졌다. 백신에 대한 불신은 백신접종의도에 영향을 미치게 된다[12]. 이렇듯 백신 안전성에 대한 문제 제기는 질병의 위험률과 유병률이 낮고 백신 프로그램이 성공적 일 때 특히 흔하게 나타날 수 있다[1]. 질병에 대한 위험성이 높지 않다고 인식되면 예방 접종을 시행해야 한다는 인지는 떨어지게 된다[13]. 반면에 인지된 질병 위험이 매우 높으면 백신의 부작용에 대한 개인들의 우려에도 불구하고 예방 접종의도가 높아 질 수 있다[14]. COVID-19 접종에 대한 의도는 폴란드의 의료인을 대상으로 시행한 연구에서 남성인 경우, 과거 백신 접종이력이 있는 경우, 자신과 가족에 대한 COVID-19의 두려움이 높은 경우와 대유행에 대한 스트레스가 COVID-19 백신에 높은 접종의도를 보였다[15]. Ledda 등[14]의 연구에서 COVID-19를 심각한 질병으로 인식하는 사람들이 그렇지 않는 사람들에 비해 COVID-19 백신접종의도가 조금 더 높았으며, 백신의 안전성, 효능에 대한 의심 및 백신에 대한 정보가 없다는 것이 COVID-19 백신접종 주저요인으로 작용하였다. COVID-19 펜데믹 초기 단계에 호주에서 연구된 바에 의하면 COVID-19 감염위험이 백신접종에 대한 결정적인 주요 예측변수가 아니라는 의견도 있었지만 독일이나 프랑스를 대상으로 시행한 연구에서는 COVID-19에 감염될 가능성이 높고 질환의 상태가 심각할수록 접종 의도가 높았다[13]. 즉 COVID-19 위험에 대한 인식이 높을수록 접종의도가 높았다고 볼 수 있다.
COVID-19 백신접종 초기 캐나다 및 이집트와 기타 국가에서 접종자를 대상으로 시행한 연구에서 백신에 대한 접종의도는 남성인 경우와 60세 이상의 경우, 그리고 COVID-19에 노출위험이 있는 경우가 높았다. 반면 백신의 효능에 대한 불신으로 인한 백신접종 저항은 백신 미접종에 영향요인으로 작용하였다[16]. 실제로 COVID-19 백신은 개발과정이 짧고 새로운 방법으로 제작되었으며 접종했던 역사가 길지 않아 안전성 부분에 대한 정보가 제한되어 접종 의사결정에 부정적 영향으로 작용할 수 있다[17]. 본 연구는 AstraZeneca (ChAdOx1) 백신을 접종해야 하는 한국의 의료기관 종사자를 대상으로 접종의도나 실태를 조사한 연구이다. 중소병원 의료기관 종사자들도 대형병원과 마찬가지로 감염병의 최전선에서 COVID-19 환자와 마주하고 집단내 감염을 경험하고 있다. COVID-19로부터 피해를 최소화 하기 위하여 적극적인 백신접종이 필요하다. 본 연구는 의료기관종사자들의 COVID-19 예방접종사례를 통하여 추후 이루어질 예방접종률을 효과적으로 향상시킬 수 있는 방법을 모색하고자 시행되었다.
2. 연구의 목적
본 연구의 목적은 300병상 모의 일개 중소 병원의 의료기관 종사자의 COVID-19 AstraZeneca (ChAdOx1) 백신접종의 영향요인을 확인하고 접종 후 이상반응의 특성을 파악하고자 하였다. 구체적인 목적은 다음과 같다
첫째, COVID-19 AstraZeneca (ChAdOx1) 백신접종 대상의 일반적 특성과 접종 실태를 파악한다.
둘째, COVID-19 AstraZeneca (ChAdOx1) 백신접종 후 이상반응의 특성을 파악한다.
셋째, COVID-19 AstraZeneca (ChAdOx1) 백신접종 시행군(Vaccinated group)과 미시행군(Non-vaccinated group) 간 접종의도의 차이를 파악한다.
넷째, COVID-19 AstraZeneca (ChAdOx1) 백신접종에 영향을 미치는 요인을 규명한다.
연구 방법
1. 연구설계
본 연구는 일 중소병원에서 COVID-19 AstraZeneca (ChAdOx1) 백신접종을 시행한 의료기관 종사자를 대상으로 COVID-19 백신접종 영향요인과 접종 후 이상반응의 특성을 파악하기 위해 시행한 서술적 조사연구이다.
2. 연구대상
연구대상은 경기도 SH시에 재한 300병상 규모의 일개 중소병원에 근무하며 COVID-19 관련 업무에 참여했던 정규 및 비정규직 의료기관 종사자로 COVID-19 AstraZeneca (ChAdOx1) 백신접종 예정이었거나 백신이 완료된 자를 대상으로 하였다. 전체 대상자수 670명 중 302명이 연구에 참여하였으며 65세 이상으로 백신접종 제외대상에 해당하는 1부를 제외한 301명을 분석하였다. 연구 대상자의 모집은 관리자를 통한 공지 후 URL에 직접 접속하여 자발적 참여가 가능하도록 하였다. 백신접종 대상자는 질병관리청의 결정에 따라 접종이 결정된 의료기관 종사자를 의미하며 연구자의 편의대로 임의대상자를 산출할 수 없었다.
3. 연구도구
1) 대상자의 일반적 특성
Kwok 등[19]이 홍콩 간호사를 대상으로 인플루엔자 백신접종, COVID-19 백신접종의도 및 주저에 대하여 조사한 연구를 바탕으로 일반적 특성은 근무부서, 직종, 연령, 성별, 과거 질환, 과거 백신접종 후 이상반응경험유무, COVID-19 백신접종의도, COVID-19 백신접종 유무, 접종사유 및 미접종 사유에 대하여 조사 하였다.
2) 접종 후 이상반응
COVID-19 백신접종 후 반응에 대하여 시행한 Kim 등[9]의 연구를 기반으로 접종 후 이상반응 유무를 기록하도록 하였고 발현시기와 소실시기를 선택하도록 하였다. 이상반응 증상은 질병관리청[20]에서 제공한 예방 접종 후 이상반응의 종류를 참고로 국소반응, 신경계반응, 전신반응 및 근·골격계 반응으로 분류하였다. 증상 중 발열여부를 제외한 나머지 이상증상에 대하여는 중복 선택이 가능하도록 하였다[18]. 접종 후 업무수행 지장 정도는 연구자가 개발하였으며, 지장을 주는 정도에 따라 1점에서 10점까지 라이커트척도로 ‘지장을 주지 않는다’ 1점에서 ‘지장을 가장 많이 준다’를 10점으로 하였다.
4. 자료수집
자료는 IRB승인 후 5월 25일부터 31일까지 일주일간 대상자가 URL을 직접 접속하여 자발적으로 참여하는 방식으로 수집하였다. 국내 의료기관의 접종은 2021년 3월 4일부터 시작되었으며, 자료수집 당시는 COVID-19가 유행하는 시기로 국내 일일당 300-400여명 대의 확진자가 발생하고 있었다[18]. 해당 병원 내 직원들은 COVID-19 집단 확진 사례를 경험하였으며, 국내 전체의료진의 우선 접종을 시작하였다. 설문지의 작성은 약 5분가량이 소요되었다. 설문지는 Google 설문지프로그램을 이용하였으며 설문이 마무리된 후 연구자가 설문을 마감하여 연구기간이 만료 후에 접속이 이루어지지 못하도록 하였다.
5. 자료분석 방법
수집된 자료는 SPSS WIN 25.0 (IBM Corporation, Armonk, NY, USA)을 분석에 이용하였다. COVID-19 백신접종 실태는 빈도와 백 분율을 이용하였으며, 백신접종 시행군과 미시행군 간 비교는 각 설명변수에 대한 이변량 단순로지스틱회귀분석(simple logistic regression)을 실시하였고 오즈비(OR)와 95%신뢰구간(confidence interval)을 산출하였다. 연령은 연속변수로 평균과 표준편차를 산출하고 연령대별 영향요인을 확인하기 위하여 연령대별로 분류하였다. COVID-19 백신접종 영향요인 확인은 백신접종 시행군과 미시행군 간 유의수준 .05에서 유의한 차이를 보인 변수들을 설명변수로 하고 COVID-19 백신접종여부를 반응변수로 하였으며, 입력(enter)방법을 이용한 다중 로지스틱회귀분석(multiple logistic regression)을 실시하였다. 로지스틱회귀분석에서 유의수준은 .05로 하였으며, 각 요인별 오즈비(OR)와 이의 95%신뢰구간을 산출하였다.
6. 윤리적 고려
본 연구는 G대학 생명윤리 심의 위원회 심의(1044396-202105-HR-093-01)를 받아 시행되었다. 연구의 대상자는 일 중소병원에 근무하는 의료기관 종사자로 서면을 통해 병원장의 허락을 득한 후 연구의 목적과 방법, 연구윤리에 대하여 설문에 직접 기재하였고 부서의 관리자들에게 설명하였으며 대상자의 참여는 웹으로 시행하여 자율성과 선택권을 고려하여 자료를 수집하였다. 연구내용에는 사생활에 침해를 일으킬 수 있는 개인정보는 포함하지 않았으며 자료의 보안을 위하여 설문 종료 후 사이트의 접속을 차단하였다.
연구 결과
1. 대상자의 일반적 특성
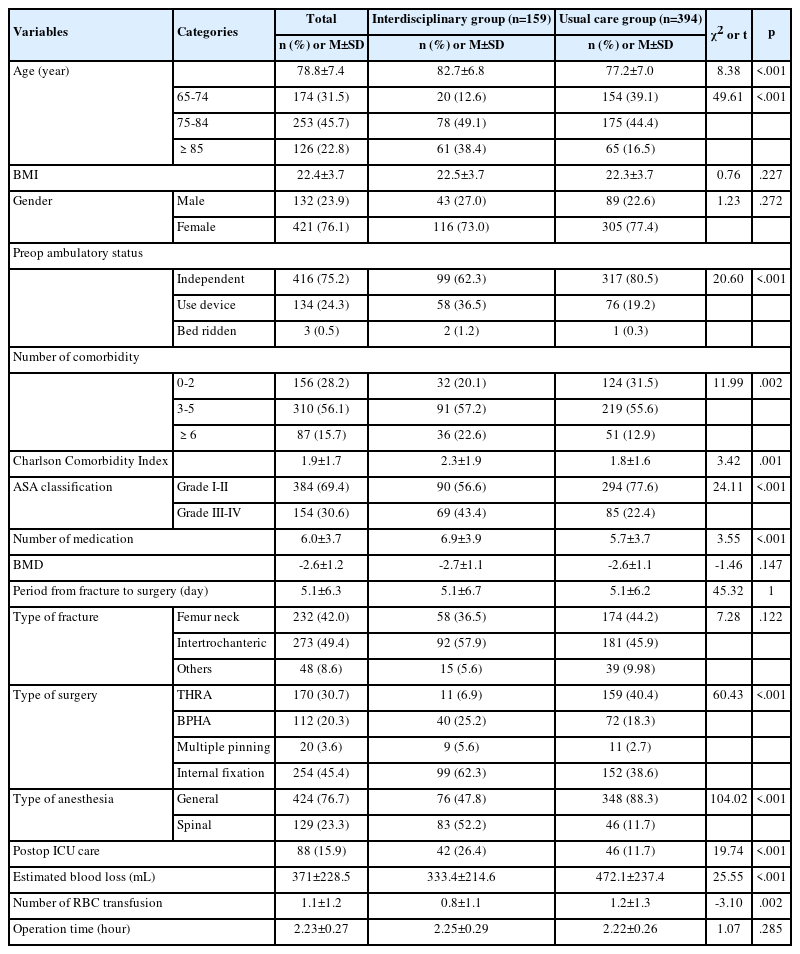
대상자 총 301명 중 남자가 15.9%, 여자가 84.1%이었고 평균 연령은 39.02±11.68이었다. 근무 형태는 임상이 75.4%, 행정이 18.6%, 지원인력이 6.0%를 차지하였다. 직종은 의사가 4.3%, 간호사가 45.2%, 간호조무사나 간호보조 인력이 25.6%였고 행정지원이 9.3%였다. 응답자 중 79.1%가 만성질환이 없다고 답하였고 20.9%는 만성질환을 보유하고 있다고 답하였다. 전체 대상자의 9.6%가 과거 다른 백신접종 후 이상반응 경험이 있다고 응답하였다.
전체 응답자 301명 중 85.7%에 해당하는 258명이 COVID-19접종을 시행하였으며 미접종자는 14.3%인 43명이었다. 전체 대상자 301명 중 268명(89.0%)이 접종이 필요하다고 응답하였고 33명(11%)은 접종이 필요없다고 응답하였다. 미접종 사유로는 이상반응에 대한 두려움이 85.7%, 임신이나 기저질환 등의 개인적인 사정이 8.6%, 백신에 대한 정보 부족이 7%, 막연한 불안감이 7%, 백신이나 정부에 대한 불신이 4.6%였고 백신종류의 선택불가가 7%였다. 접종사유는 의료기관 종사자로서의 책임감이 43.8%, 개인의 COVID-19 감염예방이 34.5%, 기관이나 부서장의 권고가 20.2%였으며, 보호장구 착용과 지역이동 불가 등의 규제완화라는 답변이 1.6%였다(Table 1).
2. COVID-19 AstraZeneca (ChAdOx1) 백신 접종 후 이상 반응
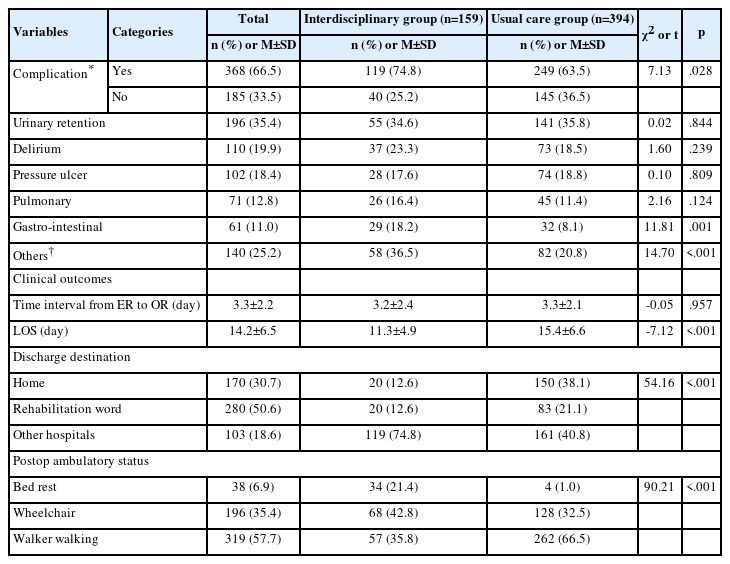
접종 후 183명이 이상반응이 있었다고 보고하였고, 이는 전체 접종인원의 70.9%에 해당한다. 이상반응 보고자 중 COVID-19 접종 후 30.6%가 이상반응 치료를 위해 진료를 받았다. 증상발현은 COVID-19 백신접종 후 38.8%가 12시간 이내였고, 50.3%가 12-24시간 이내로 가장 많았다. 이상반응증상 지속시간은 접종 후 18.6%가 24시간 이내 소실되었으며, 24-36시간 안에 61.7%가 소실되었다. 48-72시간 이내 증상이 소실된 경우가 9.3%였으며 72시간이 지나서도 증상이 지속된 경우가 10.4%였다.
이상반응 분류별 총 이상반응 중 발열은 15.8%, 국소반응 27.6%, 신경계반응 31.6%, 전신반응 4.6%, 근골격계 반응 20.4%를 차지하였다. 이중 발열을 제외하고는 중복선택이 가능하도록 하였다. 국소반응 이상부분에서 9.7%는 증상이 없었고 접종부위 통증이 51.1%, 접종부위 열감이 29.1%, 접종 인접부위 부종을 2.6%, 기타가 7.5% 보고되었다. 신경계반응 이상을 보고한 사람 중 9.8%가 없다고 했으며, 두통 36.8%, 어지러움증이 29.7%, 숙취와 같은 느낌이 18.2%였으며, 떨림이 1.8% 및 기타가 4.2%였다. 전신반응은 78.5%가 없다고 보고하였으며, 전신두드러기가 1.1%, 안면부종 3.2%, 호흡곤란 4.8% 및 기타가 12.4%였다. 2.2%가 근·골격계이상 반응이 없다고 보고하였으며, 단순근육통이 44.3%, 심한 근육통이 1.1%,. 근관절통 모두 발생한 경우가 50.3%였고 2.2%는 단순 관절통이었다. 업무에 지장이 있었는지에 대한 정도는 10점 만점에 평균 7.08±2.26이었다(Table 2).
3. COVID-19 AstraZeneca(ChAdOx1) 백신 접종군과 미접종군 간의 접종의도 차이
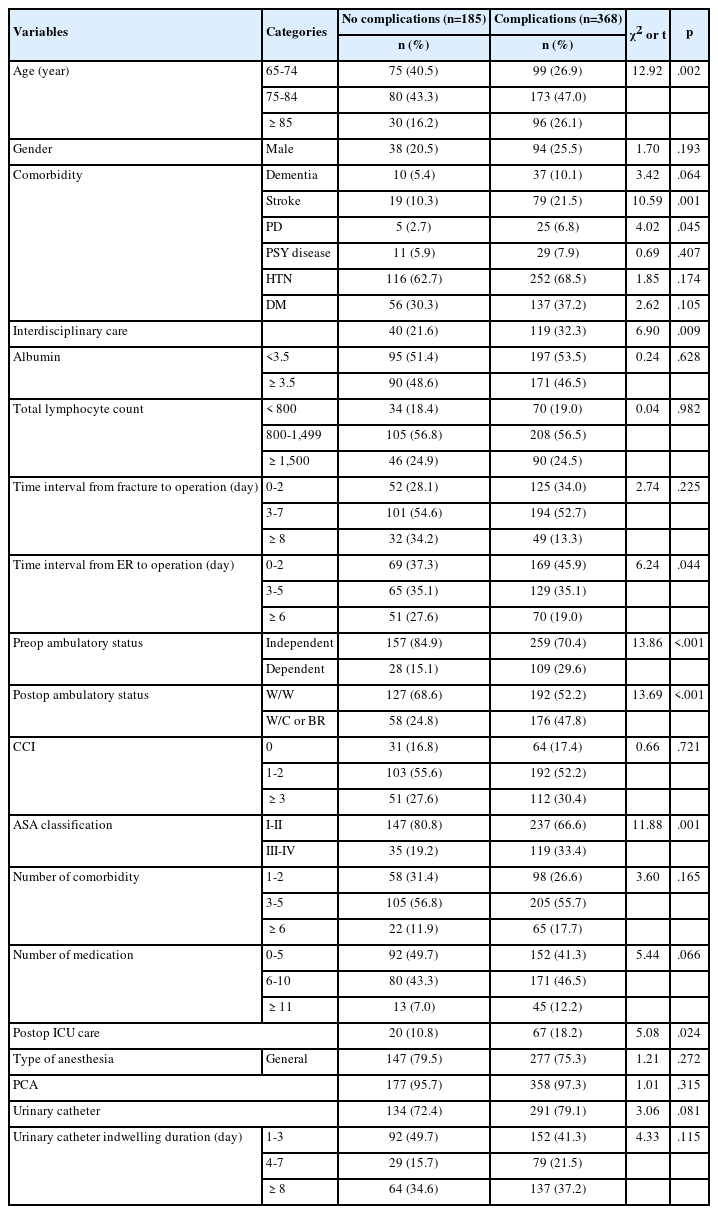
COVID-19 AstraZeneca (ChAdOx1) 백신 접종군과 미접종군의 차이는 직종에 있어 간호조무사 및 간호보조, 행정 및 지원파트에서 유의한 차이를 보였고, 연령, 과거 백신접종이상 경험, COVID-19 백신접종의도에서도 유의한 차이를 보였다(p<.05). 간호조무사와 간호보조인력은 의사보다(Odds Ratio, OR=2.94, p=.024) 백신접종률이 높았고, 행정 및 지원인력은 의사보다(OR=0.37, p=.024) 낮았으며 접종에 유의한 차이를 보였다. 연령평균은 39.2±11.68로 유의한 차이를 보였고, 연령대는 50대 이상에서 20대보다(OR=3.70, p<.011) 높았고, 유의한 차이를 보였다. 만성질환에서 과거력이 없는 군에 비해 있는 군의 접종이(OR=1.19, p=.686) 높았으나 유의한 차이를 보이지 않았다. 과거 다른 백신접종 시 이상을 경험했던 군 에 비해 과거 백신접종 이상경험이 없었던 군이(OR=3.81, p=.003) 높았으며 유의미한 차이를 보였다. 백신접종 의도는 필요 없다고 답한 군에 비하여 필요하다고 응답한 경우가(OR=8.40, p<.001) 접종률이 높았으며 유의한 차이를 보였다(Table 3).
4. COVID-19 AstraZeneca (ChAdOx1) 백신접종에 영향을 미치는 요인
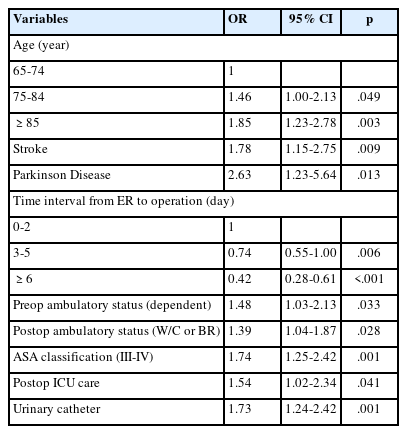
중소병원 근로자의 COVID-19 백신접종에 영향을 미치는 최종요인은 직종, 과거 백신접종 시 이상 경험, 연령, 백신접종의도였다(p<.05). 직종에서는 행정 및 지원인력이 의사직에 비하여 0.20배 접종을 적게 하였으며(p=.003), 과거접종 시 이상경험이 있었던 그룹보다 이상경험 이 없었던 그룹이 접종이 높았다(OR=3.40, p=.012). 연령은 증가시마다 접종이 증가하였으며(OR=1.05, p=.025), 백신접종이 필요하다고 응답한 군의 접종이 높았다(OR=6.66, p<.001) (Table 4).
논 의
본 연구는 COVID-19 백신접종 시 AstraZeneca (ChAdOx1)로 백신의 선택이 제한적이었던 의료기관의 종사자를 대상으로 백신접종의 영향요인을 탐색하고, 접종 후 이상반응을 조사하였다는데 그 의의가 있다. COVID-19 예방 접종이 시작되었을 당시 근로자 본인의 접종의사결정을 할 수 있는 시간이 짧았고, 정확한 정보를 인식하기도 전에 백신접종이 진행되었다는 부분과 접종 당시 국내 확진자가 일당 약 300-400명이었으며, 지속적으로 해당의료기관에서도 확진자가 발생하고 있었던 부분을 COVID-19에 대한 불확실성이 컸던 사회적 상황에 대한 고려가 필요하다[20].
본 연구에 참여한 의료기관 종사자는 접종 후 70.9%가 이상반응 을 경험하였고 이들 중 30.6%가 진료를 보았다. 접종 후 이상반응은 접종자의 주사부위 통증 등의 국소반응을 제외하고 75.4%가 이상반응이 있었고 89.1%가 접종 후 24시간 이내에 발현되었다. AstraZeneca 백신의 이상반응은 Ramasamy 등[21]의 연구에서 주사부위의 통증과 압통이 가장 흔한 이상반응이었으며 48시간 이내에 가장 많이 발생되었다. 이상반응 종류는 유사하였으나 발현시간은 선행연구보다 빠른 시간 내 발현되었음을 알 수 있었다. 접종 후 발열은 전체 대상자의 78.4%에서 있었는데 영국연방의 보고에서 41.5% [8], Kim 등[9]의 연구에서 31.2%, Bae 등[10]의 연구에서 40.9%로 본연구와 차이가 있었다. 이상반응증상 분류 4가지 중 이상반응이 없다고 응답한 경우에서 전신 이상반응 없음이 78.5%로 가장 높았고 국소 이상반응 없음이 9.7%, 신경계 이상반응 없음이 9.8%이었으며, 근관절 이상반응 없음이 2.2%로 가장 낮아 백신접종 후 이상반응 분류 중 근관절 이상반응이 가장 다빈도로 발생하였음을 유추할 수 있다. 영국연방보고서에서도 매우 흔한 증상으로 두통, 메스꺼움, 근육통과 관절통을 보고하여 본 연구와 유사함을 확인 할 수 있었다[8]. 접종 후 이상반응이 업무에 얼마나 지장을 주었냐는 질문은 본 연구에서 수행한 독자적인 질문으로 10점 만점에 평균 7.01 (±2.26)점이 업무에 지장을 주었다고 하였다. COVID-19 백신접종 후 이상반응을 고려하여 접종대상자는 충분한 수면, 휴식, 수분섭취, 금주 등 미리 건강특성에 따른 접종대상자 자체적인 준비가 필요할 것으로 사료된다. 또한 근무지나 근무부서에서는 접종 후 이상반응을 고려하여 신체강도가 높은 작업이나 야간근무 등을 피할 수 있도록 근무배정에 대한 배려가 이루어져야 할 것으로 생각한다.
본 연구에서 COVID-19 백신접종의 최종 영향요인은 직종, 연령, 과거 백신접종 이상 경험, 백신접종 의도였다. 직종별 접종에 대한 다중 로지스틱 회귀분석에서 의사에 비하여 행정직 및 지원 인력의 접종에 대한 오즈비가 0.23 (р=.007)으로 적게 나타났다. 캐나다의 의료기관 종사자를 대상으로 진행한 연구에서 직종은 접종의도의 영향 요인이 아니었으나[17], Gagneux-Brunon 등이 COVID-19유행초기 프랑스의 의료기관 종사자를 대상으로 진행한 연구에서 의사에 비하여 간호사, 간호조무사와 행정직원이 낮은 접종의도를 보여 본 연구와 일부 유사하였다[22]. 선행연구에서 이러한 차이의 원인으로 성별에 차이가 있었을 것이라 보았다. 의사직이 간호사나 조무사직보다 남성이 차지하는 비율이 높았기 때문에 해당 결과를 가져 왔다고 보았다[22]. 또한 이스라엘에 진행한 계절성 독감접종 수용에 관련된 연구에서도 간호사나 조무사직종 보다 의사의 접종률이 높았다[23]. 이는 물론 성별의 차이도 있을 것이라 여겨지는 부분도 있지만 의사직이 가진 문화와 인력 상황의 영향이 있었을 것이라 생각한다. 간호사나 간호조무사직은 다수의 근무인원이 있어 휴직이나 병가 시 인력의 대체가 의사보다 좀 더 자유롭다. 이러한 상황으로 인해 의사직은 접종에 대한 자율성을 존중하기 보다는 적극적인 접종권고로 이어졌을 것이라 사료된다. 또한 의사직에 비하여 간호사직(OR: 0.75, confidence interval, CI: 0.40-1.44), 의료기사직(OR: 0.77, CI: 0.34-1.84)과 행정직(OR: 0.37, CI: 0.15-0.9)의 접종의도가 낮았는데 이중 행정직은 의미 있는 차이(p=.024)를 보였다. 환자와 접촉시간이 길고 COVID-19 위험에 노출될 확률이 많은 직군은 높은 접종의도를 보여준다[19,21]. 행정직의 경우 진료에 직접 참여시간이나 COVID-19 환자에 노출빈도가 적어 COVID-19 위험도에 대한 인식이 높지 않았던 것으로 보인다. 또한 다른 직종에 비하여 연령이 낮은 구성원들의 분포가 많은 것도 접종의도가 낮은 사유로 고려하여 볼 수 있다[19,25]. COVID-19는 지역사회를 중심으로 감염유행이 되고 있으므로 임상을 접할 기회가 적은 행정직의 경우 감염위험에 대한 인지정도를 확인할 필요가 있다. 낮은 위험인지는 감염성 질환의 이환우려가 커진다. 감염성 질환의 이환을 예방하기 위하여 사회적 거리두기 및 방역대책 준수와 함께 예방접종의 중요성을 강조하여 인식을 변화시키려는 조직 내 노력이 필요하다. 행정직을 대상으로 신종 감염병에 대한 백신접종률 향상을 위하여 환자접점에서 근무하는 직원들의 경험을 공유하고 COVID-19 위험성과 의료기관내 전파 시 영향과 위험성을 인식시킬 필요가 있다고 생각한다.
백신 접종은 다중로지스틱회귀분석에서 연령에 따라 의미 있는 증가를 보였다. 연령대 접종을 분석한 결과 20대에 비해 50대 이상에서 OR (95%CI) 3.70 (1.28-10.74)으로 나타났다. 뉴질랜드와 미전역을 대상으로 조사한 연구에서 COVID-19 백신에 대한 접종의도 및 주저요인에 대한 조사연구에서 연령은 의미 있는 차이를 보이지 않았지만[26,27], 캐나다 의료기관 종사자를 대상으로 진행한 연구에서 50대(p=.02)와 60대(p<.001)에서 30세 미만의 연령대보다 오즈비가 1.62-3.28배 높은 결과를 보였는데 이는 본 연구와 유사하였다[17]. 프랑스 의료기관 종사자를 대상으로 진행한 연구에서도 연령이 증가할수록 접종의도 또한 증가함(p=.005)을 보였다[19,25]. 연령이 증가할수록 건강에 대한 민감성이 증가함을 알 수 있다. 또한 선행연구에서 COVID-19 환자의 사망률 예측인자로 고령(adjusted odds ratio [aOR], 1.079; 95% CI, 1.064–1.095), 남성(aOR, 1.607; 95% CI, 1.002-2.576), 고혈압(aOR, 3.576, 95% CI, 1.694-7.548), 당뇨(aOR, 12.234; 95% CI, 4.126-36.272)가 코로나19 환자의 사망 위험인자로 확인되었다[28]. 젊은 층의 경우 회복력이 빠르고 기저질환을 보유한 경우가 많지 않아 질환에 이환되더라도 큰 영향을 미치지 않을 것이라는 사고가 내면에 깔려 있을 것이라고 생각한다. 또한 고연령에 비하여 질환에 대한 위험도 인식보다는 백신의 부작용에 대한 위 험도를 높게 인식할 것으로 생각한다. 추후 백신접종 관련하여 연령이가 적을수록 접종률이 떨어지는 것을 예방하기 위하여 젊은 연령층을 겨냥하여 홍보를 특화할 필요가 있을 것으로 생각한다.
성별과 관련된 COVID-19 백신접종 시행 결과(p=.949)는 유의미한 차이를 보이지 않았다. 미국전역의 일반인 672명을 대상으로 시행한 성별에 따른 접종 의도는 의미 있는 차이를 보이지 않았고[29] 홍콩간호사를 대상으로 COVID-19 백신과 인플루엔자 접종을 비교하여 COVID-19 백신에 대한 접종의도를 조사한 연구도[19] COVID-19 백신접종의도에 성별의 차이는 없어 본 연구와 같았다. 그러나 사우디아라비아 의료기관 종사자, 프랑스 의료기관 종사자, 캐나다 의료기관 종사자를 대상으로 COVID-19 백신접종 의도를 조사한 연구에서 성별이 의미 있는 차이를 보였고 주로 남성이 여성에 비하여 접종의도가 높았다[24-26,30,31]. 의료기관은 일반 타직종에 비하여 여성이 차지하는 비율이 높다. 의료기관 종사자를 대상으로 진행된 다수의 연구에서 남성이 여성보다 접종의도가 높은 것을 단순히 남성이 사회적인 진출이 많아서라는 사유로 단정하기에는 한계가 있다. 여성이 느끼는 백신에 대한 부작용 및 위험도에 대한 민감도의 차이가 있을 것으로 생각된다. 선행연구를 통하여 유행성 인플루엔자의 접종 시 일반적으로 남성의 접종수용도가 여성보다 더 높은 것을 알 수 있다[25]. COVID-19 백신도 접종 후 통증이나 부작용 발현에 대한 불안도가 남성에 비하여 여성이 높기 때문에 접종 의도나 접종에 차이가 있었을 것이라 사료된다. 또한 COVID-19 사망률에 대한 성별의 차이가 접종률에 영향을 주었을 가능성도 있다[28]. 여성에 비하여 높은 남성사망률은 백신의 잠재적 부작용에 대한 위험도보다 예방할 수 있는 질환에 대한 안전성에 우선순위를 두었을 것이라 생각한다.
본 연구에서 가장 높은 백신 접종사유는 의료기관 종사로서의 책임감(43.8%)으로 조사되었다. 이는 홍콩간호사[19]와 영국의 의료기관 종사자를 대상으로[32] 시행한 연구와 영향요인이 유사하였다. 홍콩간호사를 대상연구에서 COVID-19 백신접종의도에 집단적 책임이(OR 2.43, p<.001) 의미 있는 차이를 보였고[19], 영국의 의료기관 종사자를 대상으로 한 연구에서 COVID-19에 대한 위험성보다는 다른 사람을 보호하기 접종의도가 의미 있는 차이를 보였다[32]. 이는 COVID-19 환자를 직접 다루는 의료기관이나 그에 종사하는 구성원으로서 집단적 책임감과 부담감을 느꼈을 것으로 판단된다. 다른 백신접종에 비하여 개인적인 의도의 영향보다는 팬데믹 상황에 의료기관 종사자들이 느끼는 의료인으로서 사회적이고 대의적인 책임감이 작용한 것으로 사료된다. 그럼에도 불구하고 선행연구에서 일반인에 비하여 의료기관 종사자들의 백신접종 수용 의도가 낮음을 알 수 있다[9,32]. 이에 의료기관 종사자의 접종률을 올리기 위하여 의료기관 종사자로서 집단적 책임감을 확인하고 강화할 방법에 대한 모색이 필요가 있다. 신종감염병에 대한 의료기관 종사자들의 책임감에 영향을 주는 요인들에 대한 연구가 현재는 미비한 상황이다. 이를 확인하기 위한 질적연구방법론을 통한 탐구가 필요할 것으로 생각한다.
본 연구에서 주요 백신의 접종 사유 중 의료인으로서의 책임감을 제외하고 기관과 부서장의 권고와 COVID-19 감염에 대한 두려움 있었다. 이는 조직과 부서의 문화가 백신접종에 긍정적인 방향으로 형성되어야 하며 COVID-19 감염병 위험도에 대한 정확하고 객관적인 정보를 제공해야 할 것이다. 그리하여 감염병 위험도에 대한 인식을 높여 백신접종에 대한 의도를 향상 시킬 수 있는 방법을 모색해야 할 것으로 생각한다.
과거 백신접종 이상반응경험은 백신접종의사결정에 영향을 미치며 과거백신접종 이상반응경험이 있었던 사람에 비해 없었던 사람이 3.396 (p=.0.12)배 더 높은 접종을 보였다. 과거 접종한 백신에 대한 이상반응경험과 COVID-19 백신접종 관련 연구는 찾을 수 없었으나 인플루엔자 접종에 대한 부정적인 태도는 백신접종의 주요한 장애 요인이었다[25,33]. 과거 백신접종 시 이상반응을 경험한 경우 백신접종에 대한 부정적인 태도를 갖게 된 것으로 보인다. 백신접종률 향상을 위하여 백신접종 시 이상반응경험이 있었던 사람은 사전에 접종예진 시 관련 정보에 관한 세심한 청취가 이루어져야 한다. 또한 백신접종 후 이상반응에 영향을 줄 수 있는 환경적 요인을 미리 통제하는 것도 필요할 것으로 생각한다. 의료진은 백신접종 이상반응에 대한 사전평가를 통하여 접종을 시행여부를 명확하게 판단하고 환자에게 이상반응증상에 대하여 미리 정보를 제공하고 교육하여 증상발현 시 빠른 조취를 취해야 한다. 이때 간호사는 소통의 매개이며 상담가와 관리자로서 역할의 중요성을 시사한다.
COVID-19 백신접종의도를 가진 군은 그렇지 않은 군에 비하여 백신접종이 6.664 (p<.001)배 많았다. 이는 COVID-19 접종에 가장 큰 영향을 주는 요인이었다. 기존 연구에서 접종의도는 나이, 교육정도, 환자의 직접치료에 참여한 의료인, COVID-19에 대한 두려움, 과거 백신접종 준수, 다른 사람의 권유 등이었다[10,16,34,35]. 해당 결과들이 본 연구결과와 유사함을 알 수 있었다. COVID-19 접종의도는 접종시행 전에 백신접종을 예측하기 위한 최종 결과변수였기에 CODID-19 백신접종의도 영향요인들로 밝혀진 연구들을 비교하고 분석하여 앞으로도 발생 가능한 신종 감염병의 발현 시 접종 대책을 세울 때 적용이 가능할 것이라 생각한다. 해당 연구 결과들을 바탕으로 백신접종의도에 영향을 주는 요인들[10,14,18,21,32-36]을 개선하는 전략적 접근이 이루어져야 하겠다.
본 연구에서 COVID-19 백신의 접종 거부 요인이 백신의 부작용 에 대한 신뢰 문제가 58.1%로 가장 높았다. 캐나다 의료기관 종사자를 대상으로 시행한 연구에서 백신의 거부 사유가 신규백신이라는 것에 대한 두려움이 있었고 다른 사람들이 먼저 접종 시행 후 부작용 추이에 확인하고 접종하기를 원하였으며, 또한 의사결정의 시간이 부족함을 꼽았다[15]. 홍콩과 프랑스 간호사를 대상으로 한 연구에서는 의료기관 종사자의 COVID-19 백신접종 수용의도 수준은 낮았다[18,30]. 이러한 의료기관 종사자의 불신과 불안은 일반인들의 접종의도에 영향을 줄 수도 있다. 따라서 COVID-19 백신 접종 주저나 수용 관련된 요인들을 파악하여 의료기관 종사자들의 백신접종 수용을 늘리는데 활용해야 할 것으로 생각한다. 정부는 포탈을 통해 COVID-19와 백신에 대한 많은 정보를 제공하고 있다[19]. 그러나 의료기관 종사자들이 해당 정보를 받아들여 COVID-19 백신접종을 수용하기까지 물리적이면서 통합적인 과정이 필요하다. 불신과 불안이 높은 의료기관 종사자를 위하여 의무적 사전교육 후 백신 접종 수용에 대한 의사결정이 이루어지는 과정을 진행하는 부분도 고려가 가능할 것이다. 이러한 통합적인 과정을 끌어가는데 간호사는 리더로의 위치에 서고 교육자로의 역할을 감당하는데 간호학적 의의가 있을 것으로 생각한다.
본 연구의 제한점은 연구대상자가 국내 일개 중소병원의 의료기관 종사자로 전체 의료기관을 대표하지 못하며, 백신 접종이 이루어진 이후 조사되었고 단일약제(AstraZeneca-ChAdOx1) 접종관련 대상자만 조사하였다는 점이다. 따라서 COVID-19 백신의 종류에 따른 다양한 접종 영향요인에 대한 분석이 추후 필요하다고 본다. 또한 향후 대상자수를 확대하여 백신접종의도 영향요인에 대한 결과를 검증할 것에 대한 추가연구와 감염관리에 대한 조직의 태도, 리더쉽과 정책이 접종의도에 어떠한 영향을 주었는지 규명을 위한 연구를 제언하는 바이다.
결 론
본 연구는 일 중소병원의 의료기관 종사자를 대상으로 COVID-19 AstraZeneca (ChAdOx1) 백신 접종에 영향을 미치는 요인과 이상반응의 실태를 파악하였다. 대상자에 대한 정보를 능동적으로 수집하여 백신접종 당시 이상 반응경험을 파악하는 것은 발생 가능한 이상반응에 대한 준비를 사전에 대비할 수 있다. COVID-19 백신접종에 영향을 미치는 위험요인은 접종의도, 과거 다른 백신접종 부작용 경험, 직종, 연령이었다. 특히 COVID-19 백신접종 향상을 위하여 접종이 저조한 직군인 행정직과 낮은 연령의 종사자 및 과거 백신접종부작용 경험자들에 대한 맞춤별 홍보와 적절한 정보제공 및 체계적인 교육이 이루어져야 할 것이다. 이상의 결과를 바탕으로 앞으로 확대될 COVID-19 백신접종과 새로운 신종 감염병 발현 시 이루어질 백신접종 관련하여 참고 자료로 사용되어 지기를 기대한다.
CONFLICT OF INTEREST
The authors declared no conflict of interest.
AUTHORSHIPS
LSH contributed to the conception and design of this study; LSH collected data; CJS & LSH performed the statistical analysis and interpretation; CJS & LSH drafted the manuscript; CJS & LSH critically revised the manuscript; CJS supervised the whole study process. CJS & LSH authors read and approved the final manuscript.