MPTP로 유도된 신경 독성에 대한 NXP031의 개선 효과
Ameliorative Effects of NXP031 on MPTP-Induced Neurotoxicity
Article information
Abstract
Purpose: The purpose of this study was to investigate effects of NXP031, an inhibitor of oxidation by specifically binding to the complex of DNA aptamer/vitamin C, on dopaminergic neurons loss and the reaction of microglia in an animal model of 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine (MPTP)-induced subchronic Parkinson’s disease (PD). Methods: A subchronic PD mouse model was induced via an intraperitoneal (IP) injection of MPTP 30 mg/kg per day for five days. NXP031 (vitamin C/aptamer at 200 mg/4 mg/kg) and vitamin C at 200 mg/kg were administered via IP injections at one hour after performing MPTP injection. This process was performed for five days. Motor function was then evaluated with pole and rotarod tests, after which an immunohistochemical analysis was performed. Results: NXP031 administration after MPTP injection significantly improved motor functions (via both pole and rotarod tests) compared to the control (MPTP injection only) (p<.001). NXP031 alleviated the loss of dopaminergic neurons in the substantia nigra (SN) and striatum caused by MPTP injection. It was found to have a neuroprotective effect by reducing microglia activity. Conclusion: NXP031 can improve impaired motor function, showing neuroprotective effects on dopaminergic neurons in the SN and striatum of MPTP-induced subchronic Parkinson’s disease mouse model. Results of this study suggest that NXP031 has potential in future treatments for PD and interventions for nerve recovery.
서 론
1. 연구의 필요성
파킨슨 병(Parkinson’s disease, PD)은 대표적인 신경퇴행성 질환으로 진전, 근육의 강직, 운동 서완을 특징으로 하며[1], 장애의 수준이 높아질수록 우울, 불안, 수면 장애 같은 비 운동성 합병증 또한 크게 증가하여 환자 뿐만 아니라 돌봄 가족의 전반적인 삶의 질에 영향을 미치게 된다[2]. 2003년에서 2014년 까지의 국민건강보험공단 자료 분석에 의하면 우리나라의 PD 유병률과 발생률은 꾸준하게 증가하고 있으며 특히 고령에서 높은 증가율을 보이고 있다[3].
PD의 주된 병리 현상은 중뇌의 흑질 치밀부(substantia nigra pars compacta, SNpc)의 멜라닌 색소를 함유한 도파민성 신경의 세포 사 멸과 선조체와 흑질 사이의 도파민 신경전달 물질의 결핍, 그리고 α-synuclein이 다른 단백질들과 응집되어 있는 루이소체라는 비정상적인 단백질의 존재를 특징으로 한다[4]. PD의 운동 실조의 원인은 흑질의 도파민 신경세포의 상실로 인해 운동신경의 자극이 감소되어 일어나는 것으로 알려져 있으며[5] PD 환자의 사후 부검 분석에 의하면 흑질의 50-70%, 선조체의 도파민은 80%가 사멸된 상태에서 임상증상이 발현되었다[6]. 그러므로 PD는 조기 발견과 기능 유지를 위한 치료법이 중요하다고 할 수 있다.
PD의 사례 중 유전성은 10% 미만으로 비교적 낮으며 살충제, 제초제 같은 독성물질이나, 자동차 배기가스나 공해 등에 의한 환경적 요인의 가능성이 제기 되었으나[7] 아직까지 그 원인이 정확하게 밝혀지지는 않았다. 과도한 활성산소종(reactive oxygen species, ROS)의 생성에 의해 유도되는 산화 스트레스는 PD 발병의 주요 원인으로 가정된다[8]. 산화 스트레스는 ROS의 생성과 세포의 항산화 기전의 균형이 깨질 때 발생하며 세포 손상을 일으키는 위험한 상태로 많은 질병에서 해로운 영향을 미친다[9]. 산화스트레스로 손상된 도파민 신경세포는 도파민 대사 과정에서 시냅스 소포 외부로 과도한 양의 도파민을 방출하고 효소대사에 의해 도파민 산화를 활성화한다. 도파민 자체의 독성은 없지만 도파민 대사 산물은 monoamine oxidase (MAO)에 의해 H2O2를 생성하며 도파민 산화과정에서 2개의 수산기 그룹에 있는 전자와 양성자는 산소로 이동하여 superoxide radical를 생성하여 도파민 신경세포를 손상시킨다[10].
PD의 치료는 신경화학적 특징을 기초로 하여 혈액-뇌 장벽을 통과할 수 있는 도파민의 전구체인 레보도파 요법으로 시작하였다[11]. 하지만 레보도파의 장기간 사용은 약물 치료의 효과를 떨어뜨리거나 이상 운동 항진이라는 또다른 부작용 가능성이 높아져[12] 증상을 완화시키지만 근본적인 치료의 한계를 나타내고 있다. 최근에는 2형 당뇨병 치료제로 사용되는 glucagon-like peptide-1 receptor (GLP-1) 유사체가 세포 및 동물 모델에서 신경 보호 효과를 나타내는 것으로 밝혀진 후 PD 환자에서 임상시험이 진행되고 있다[13-15]. 또한 PD의 병리적 특징인 α-synuclein의 비정상적인 응집을 제한하는 항체를 사용하는 면역요법[16], 그리고 줄기세포를 이용한 치료제가 개발되고 있으나[17] 아직까지 어떠한 새로운 치료법도 효과를 입증하지는 못하고 있다.
PD의 병리적 변화를 확인하기 위해서는 사람의 사후 뇌 조직을 건강한 뇌와 비교를 해야 하는 어려움이 있으며 질병의 원인과 새로운 치료법의 확인을 위해서는 동물 모델에서의 실험결과가 선행되어야 한다. PD 동물 모델은 신경 독성 모델과 유전자 변형 모델로 나눌 수 있으나 유전학적 모델의 경우 PD의 전형적인 병리상태인 도파민 신경세포의 사멸이 발생되지 않아 적용이 어려운 실정이다[18]. 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine (MPTP)는 1980년대 초 미국의 마약 사용자들이 meperidine의 불법 합성 과정에서 우연히 생성된 물질로 정맥주사후 급성 운동장애를 포함하는 파킨슨 증상이 산발적으로 발생하여 알려졌으며 이후 PD 모델을 위한 신경 독성 화합물로 사용되었다[19]. MPTP는 친유성이 높고 전신 주사 후 뇌-혈관 장벽을 쉽게 통과하여 별아교세포로 들어와 monoamine oxidase-B에 의해 독성 대사물인 1-methyl-4-phenyl-1,2,3,6-tetrahydropyridinium ion (MPP+)로 전환된다[20]. MPP+는 도파민 수송체에 의해 도파민성 신경세포 내로 들어와 미토콘드리아 전자전달계 중 복합체I을 억제하여 adenosine triphosphate (ATP)고갈, ROS의 과다 생성으로 이어진다[21]. 결국 도파민성 신경세포의 사멸을 가져와 특발성 PD 발병에 관여하게 되며[22] 이러한 메커니즘의 많은 부분이 파킨슨 병 환자의 발병 기전의 특징과 비교 했을 때 동물 모델 적용의 높은 타당성을 설명한다[23].
Vitamin C (L-ascorbic acid)는 대표적인 항산화제로 산화스트레스 억제, 지질의 과산화 감소, ROS를 제거하는 기능을 하고 있어 신경계의 생리기능에서 중요하다[24]. 하지만 vitamin C는 산소, 빛, 열, 물 등에 의해 쉽게 산화되어 치료제로서의 한계를 가지고 있었다[25]. Aptamer는 단일 DNA 혹은 RNA 염기 가닥으로 특정 표적 물질에 높은 특이성과 결합력을 갖는 물질이다[26]. 최근 특정 물질과 잘 결합하는 DNA aptamer (aptamin)에 vitamin C를 결합하여 기존의 vitamin C의 단점을 극복할 수 있는 물질(NXP031)이 개발되었다[27]. Song 등[28]은 NXP031을 MPTP로 유도된 급성 PD 모델에 적용했을 때 운동장애 개선과 혈장의 ascorbic acid (AA) 농도가 향상되어 흑질과 선조체의 도파민성 뉴런의 손상이 개선되었다고 보고하여 PD 치료법에 대한 새로운 제안을 제시하였다. 그럼에도 PD의 병태생리를 고려한다면 급성 독성 모델 보다 좀더 생리적인 만성 동물모델에서의 효과 확인이 필요하다고 여겨진다. 현재까지 다양한 PD 동물모델이 개발되었음에도 점진적인 신경퇴화 과정의 모델을 구축하는 것은 여전히 한계가 존재한다[29]. 이에 본 연구에서는 아만성 PD 모델을 구축한 후 NXP031를 복강내 투여하여 도파민성 신경세포 손상과 미세아교세포 반응성에 미치는 효과와 운동기능에서의 변화를 확인하고자 한다.
2. 연구 목적
본 연구는 MPTP로 유도된 아만성 파킨슨병 동물 모델에 NXP031를 복강내 투여한 후 운동기능의 향상, 뇌 흑질과 선조체에서의 도파민성 신경세포의 손상 약화, 그리고 미세아교세포 활성화 감소를 확인하여, NXP031의 신경보호 효과를 보고자 한다.
연구 방법
1. 연구 설계
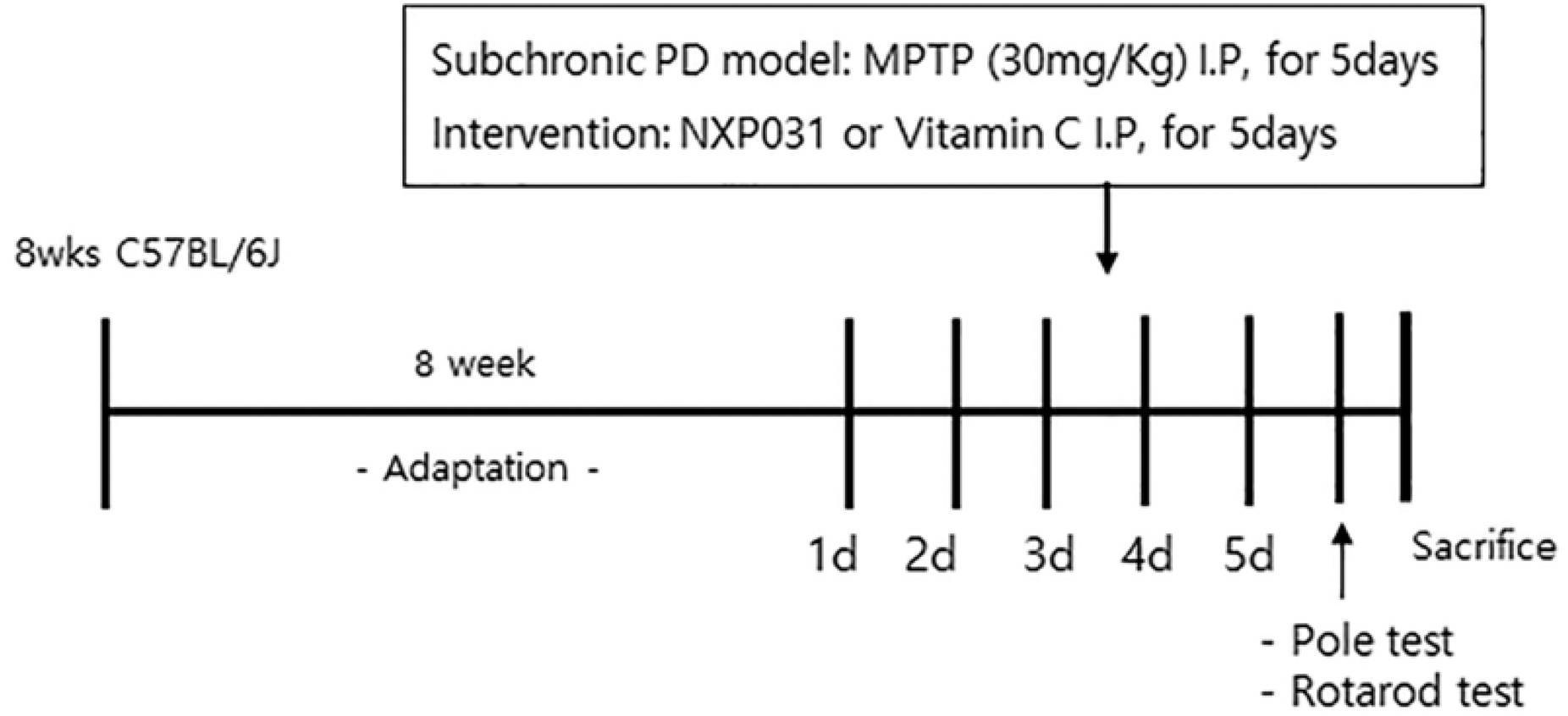
입고된 8주령의 C57BL/6J mouse는 8주동안 적응과 성숙의 과정을 거쳐 초기 성인 연령이 되었을 때 체중 1 kg 당 30 mg의 MPTP를 5일동안 복강내 투여하여 PD model을 유도하였다. 중재는 매일 MPTP 투여 1시간 후에 vitamin C (200 mg/kg)와 NXP031 (aptamin: vitamin C =4 mg: 200 mg/kg)를 복강 투여하였으며 MPTP가 투여되는 5일동안 중재 또한 지속되었다. 그룹은 모두 네 그룹으로 정상군인 Sham, MPTP만 투여되는 PD, MPTP 투여 후 Vitamin C를 투여하는 PD+VitC 그룹, 그리고 MPTP 투여 후 NXP031을 투여하는 PD+NXP031 그룹으로 배정되었다. 5일간의 모델 유발과 중재가 끝난 다음 날 행동실험으로 pole test, rotarod test를 시행한 후 희생시켜 뇌 조직을 획득하였다(Figure 1).
2. 연구 대상
1) 실험동물
C57BL/6 종은 지금까지 알려진 동물 중에서 MPTP에 가장 민감하여 PD의 치료 연구에 많이 사용되고 있다[30]. C57BL/6J 마우스 40마리를 Orient Bio (Osan, Korea)에서 제공받았다. 실험동물은 입고 후 1주일간 적응시킨 후 한 케이지당 4마리씩 사육하였다. 이후 16주령이 될 때까지 물과 사료는 자유롭게 섭취하도록 하였으며 항온, 항습이 조절되어 동물 생활하기 좋은 환경(온도 22±2°C, 습도 50±3%, light cycle 12 hr)을 유지하였다.
2) 파킨슨병 아만성 모델 유발
파킨슨병에 대한 동물 연구는 MPTP (1-Methyl-4-phenyl-1,2,3,6-tetrahydro pyridine hydrochloride) (Sigma-Aldrich, St. Louis, MO, USA)을 사용하는 마우스 모델이 가장 널리 사용된다. 본 연구에서는 급성 모델과 만성 모델의 중간격인 아만성 모델을 유발하기 위해 선행 연구를 바탕으로[31] 실험동물(28-30 g)에 MPTP (30 mg/kg, IP)를 하루에 한번씩 총 5일 동안 주사하여 PD 모델을 유발하였다. PD 급성 독성 모델에서 사용되는 MPTP 용량은 20 mg/kg 으로 하룻동안 2시간 간격으로 4번 IP 하여 유도되며[32] 본 실험의 프로토콜과는 용량과 기간에서 차이가 있다. MPTP 주사 과정에서 6마리가 사망하여 최종 Sham 그룹 10마리, PD, PD+VitC, 그리고 PD+NXP031 그룹은 각각 8마리가 되었다.
3) NXP031의 제조
Nexmos (Yongin-si, Korea) 사로부터 제공받은 50 mg의 aptamin을 1 mM MgCl2가 녹아 있는 3차 증류수에 용해시켜 사용하였다. Aptamin은 용매를 90-95°C로 가열한 뒤 첨가하여 녹였으며 이후 삼차 구조 형성을 위해 상온으로 서서히 식혀 stock을 만들었다. 이후 aptamin과 vitamin C를 1:50 비율로 혼합하여 사용하였다. Vitamin C는 증류수에 녹여 사용가능한 농도로 준비하였다. 정상군과 대조군 그룹에는 동량의 0.9%의 생리식염수를 적용하였다.
3. 연구도구 및 자료수집
1) Pole test
PD와 관련된 운동기능의 효과를 평가하기 위해 높이 55 cm, 지름 8 mm의 막대를 이용하여 pole test를 실시하였다. 실험동물의 머리가 위로 향하게 하여 막대의 맨 위에 매달릴 수 있도록 올려놓고 실험을 시작하였다. 실험동물이 막대의 꼭대기에서 바닥 쪽으로 몸을 180° 도는 행위를 turn time, 네다리 모두가 땅에 닿을 때까지 내려오는데 걸리는 시간을 total time으로 하여 기록하였다. 제한 시간은 180초로 하였으며 제 시간안에 내려오지 못하는 동물은 180초로 기록하였다. 또한 모든 실험은 동일한 프로토콜을 숙지한 2인 이상의 실험자가 3회 시행하여 평균 값을 사용하였다.
2) Rotarod test
PD와 관련된 운동 기능의 두번째 평가를 위해 rotarod test를 실시하였다. Rotarod 기구는 공중에서 움직이는 회전 봉으로 다양한 가속 속도를 조절할 수 있으며 실험 동물이 떨어지지 않고 유지하는 능력을 측정하며 운동 실조의 지표로 사용되는 검사이다[33]. 본시험에 앞서 마우스용 rotarod 기구를 이용하여 15 rpm에서 3분간 훈련하여 검사 환경과 방법에 익숙할 수 있도록 하였다. 이후 본시험에서의 제한시간은 480초로 하였으며 rpm을 달리하면서 낙하 시간을 기록하였고 3회 반복하여 평균값을 구하여 분석에 이용하였다.
3) 조직 절편의 제작
모든 실험이 종료된 실험동물은 ethyl ether (5 mL/250 g)로 흡입 마취한 후 경추를 탈골시켜 빠르고 고통없이 희생하였다. 이후 흉강을 열어 좌심실에 24G 바늘을 삽입하여 0.05 M phosphate buffered saline (PBS)으로 관류하여 혈액을 제거한 후 4% paraformaldehyde (PFA)을 50-60 mL/min의 속도로 일정하게 관류하여 조직을 고정한후 뇌를 적출하였다. 적출된 뇌는 4% PFA 용액을 이용하여 4°C에서 24시간 동안 추가 고정하였다. 고정된 뇌 조직을 30% sucrose-PBS 혼합액을 이용하여 저온에 보관하여 수분을 제거한 후 동결 절편기를(Cryostat, Leica, Nuolch, Germany) 이용하여 관상면을 30 μm 두께로 잘라 저장액에 담아 4°C에 보관하였다.
4) 면역조직화학법
면역조직화학 분석을 위해 조직 절편 중 SN 부위를 꺼내어 0.1 M PBS로 수회 세척한 후 3% 과산화 수소로 20분간 반응하여 내재성 peroxidase를 제거하였다. 다시 PBS로 세척한 후 일차 항체로 anti-tyrosine hydroxylase (TH, 1:500, Abcam, Cambridge, UK), anti-Iba1 (1:500, Abcam, Cambridge, UK)을 이용하여 4°C에서 밤새 반응시킨 후 세척하였다. 일차 항체에 맞는 이차 항체(Vector USA)를 1시간동안 실온에서 배양하여 세척한 후 차례로 avidin-biotin complex (Vector Elite ABC kit, Vector Laboratories, Burlingame CA, USA)를 1시간 반응시켰다. 마지막으로 3,3-diaminobenzidine tetrahydrochloride (DAB kit, Vector Laboratories, Burlingame, CA, USA)를 사용하여 2-5분 간 발색 시킨 후 알코올 탈수와 xylene 투명화 과정을 거친 조직을 슬라이드에 붙여 건조하였다. 이후 permount로 coverslide를 덮은 후 광학현미경(BX51, Olympus Co., Ltd., Tokyo, Japan)으로 흑질과 선조체 부위를 10X, 40X 배율로 관찰하였다. 흑질의 치밀 부위의 TH-면역양성신경세포 분석은 염색된 신경세포 수를 분석하였으며 미세아교세포의 반응성은 image J 프로그램을 이용하여 활성 면역반응의 부위의 면적(%)을 구하여 분석하였다.
4. 자료분석
모든 실험 결과는 세번 반복하여 평균값을 구하였으며 데이터는 평균과 표준 오차로 표시하였다. 통계분석은 SPSS 25 프로그램을 이용하였고 각 집단의 차이를 검정하기 위해 일원분산분석(One-way ANOVA)을 시행하였다. 사후분석은 scheffe 검정하였으며 통계적 유의성은 p<.05로 채택하였다.
5. 윤리적 고려
본 연구는 동물실험윤리위원회의 정책 및 NIH의 동물 실험에 관한 가이드를 준수하였으며 3R (replacement, refinement, reduction) 원칙에 따라 동물실험을 수행하였다. 본 연구의 참여자는 모두 동물 취급, 주사 주입 및 채혈, 그리고 마취제 투여에 대한 적절한 교육을 받았으며 모든 실험 절차는 K대학교 동물실험윤리위원회 연구 승인 후(승인번호: KHSASP-19-227) 진행되었다.
연구 결과
1. 운동장애 개선효과
첫번째 행동평가로 진행된 pole test에서 turn time (F=12.67, p<.001)과 total time (F=6.19, p=.002) 모두 그룹 간의 차이가 발생하였다. 사후 분석 결과 모두 Sham 그룹에 비해 PD 그룹에서 평균 시간이 유의하게 지연되어(p<.001) 아만성 PD 모델이 적절하게 유도되었음을 보여주었다. Vitamin C을 투여 받은 그룹은 PD 그룹에 비해 봉에서 내려오는 평균 시간은 향상되었지만 개체 차이가 심하여 통계적 유의성은 없었다. 반면 NXP031을 투여 받은 PD+NXP031 그룹은 PD에 비해 유의하게 향상되어(p<.001) turn time에서는 19배, total time에서는 5배 이상 감소하여 PD 유발로 인해 발생한 운동장애가 NXP031 투여로 향상되는 것을 알 수 있었다(Figure 2-A). 두번째 운동기능 평가로 진행된 rotarod test에서도 그룹 간에 차이가 발생하였다(F=77.55, p<.001). 사후검정 결과 Sham 그룹이 351.7초 동안 통나무 돌리기 운동을 한 것에 비해 PD 그룹은 25.6초를 기록하여 정상군에 비해 유의하게 빨리 추락하여 운동기능이 감소되는 것을 확인할 수 있었다(p<.001). Vitamin C를 투여 받은 그룹은 PD에 비해 더 오랫동안 운동하였지만(p<.001) Sham 그룹에 비해서는 감소되었다(p<.001). 한편 NXP031을 투여 받은 그룹은 PD 그룹보다 향상되었을 뿐만 아니라 vitamin C 그룹 보다도 유의하게 더 오랫동안 운동하여(p<.001) 운동기능이 회복되는 것을 보여주었다(Figure 2-B).
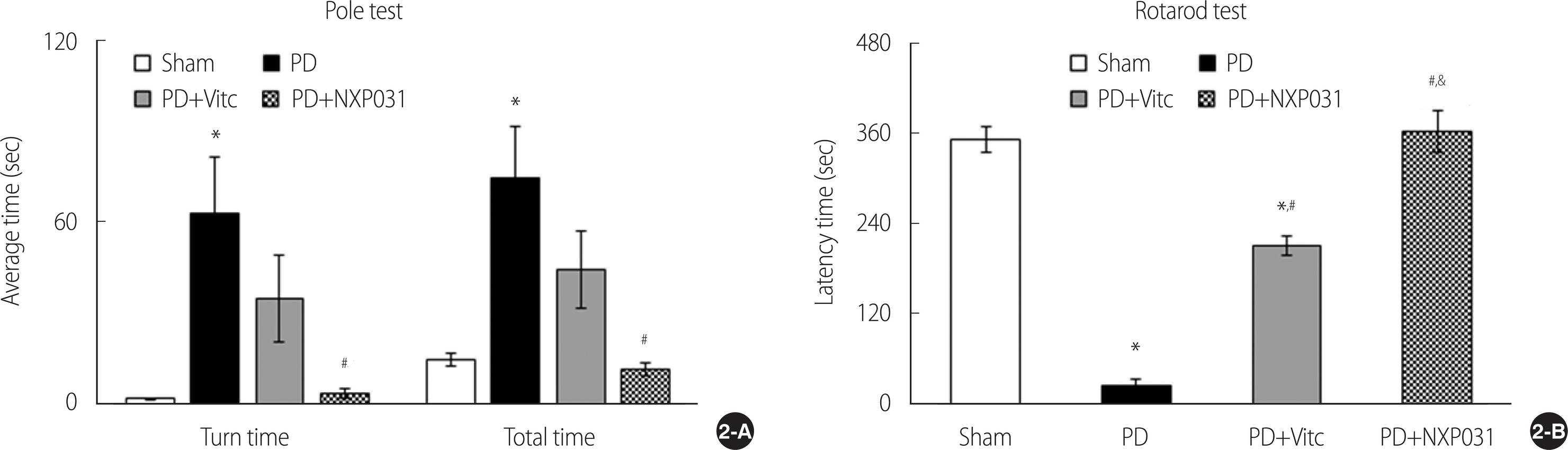
Effect of NXP031 on the motor function. Turn time (sec) and total time (sec) to descend in the pole test (A), latency time (sec) in the rotarod test (B). Data are expressed as mean±S.E.M. S.E.M: Standard error of the mean. *Significantly different from Sham, #significantly different from PD, &significantly different from PD+VitC. PD=Parkinson’s disease; VitC=Vitamin C.
2. 중내 흑질에서 도파민성 신경세포와 미세아교 세포의 활성양상
1) 도파민성 신경세포 변화
흑질 부위에서 도파민성 신경세포의 변화를 확인하기 위해 TH 항체로 반응시킨 결과 세포 수에서 그룹 간의 차이가 발생하여 사후분석을 실시하였다(F=29.21, p<.001). 정상군인 Sham은 중내 흑질 부위에 많은 양의 도파민성 세포가 확인되었으나 PD 그룹은 정상군에 비해 1/3 이상 도파민성 신경세포가 소실되었다(p<.001). PD+VitC 그룹은 PD 그룹에 비해 도파민성 신경세포가 2배 정도 회복되었으나(p=.002) Sham 그룹보다는 양성 세포수가 적었다(p=.006). 반면에 PD+NXP031 그룹은 PD 그룹에 비해 도파민성 신경세포가 약 3배정도 증가하였으며(p<.001), vitamin C 그룹에 비해서도 1.4배 정도 증가하여 통계적인 차이를 보였다(p=.019). 선조체 부위에서의 TH 면역반응 후 optical density (OD)를 분석한 결과 그룹 간 차이가 발생하였다(F=38.90, p<.001). 사후검정 결과 정상군인 Sham에 비해 PD 그룹에서 유의하게 OD가 감소하였고(p<.001), NXP031 투여 그룹만이 PD 그룹에 비해 향상되었다(p<.001). 이로써 NXP031의 복강내 투여가 흑질과 선조체 부의의 도파민성 신경세포의 손상을 감소시키는 것을 확인 할 수 있었다(Figure 3).
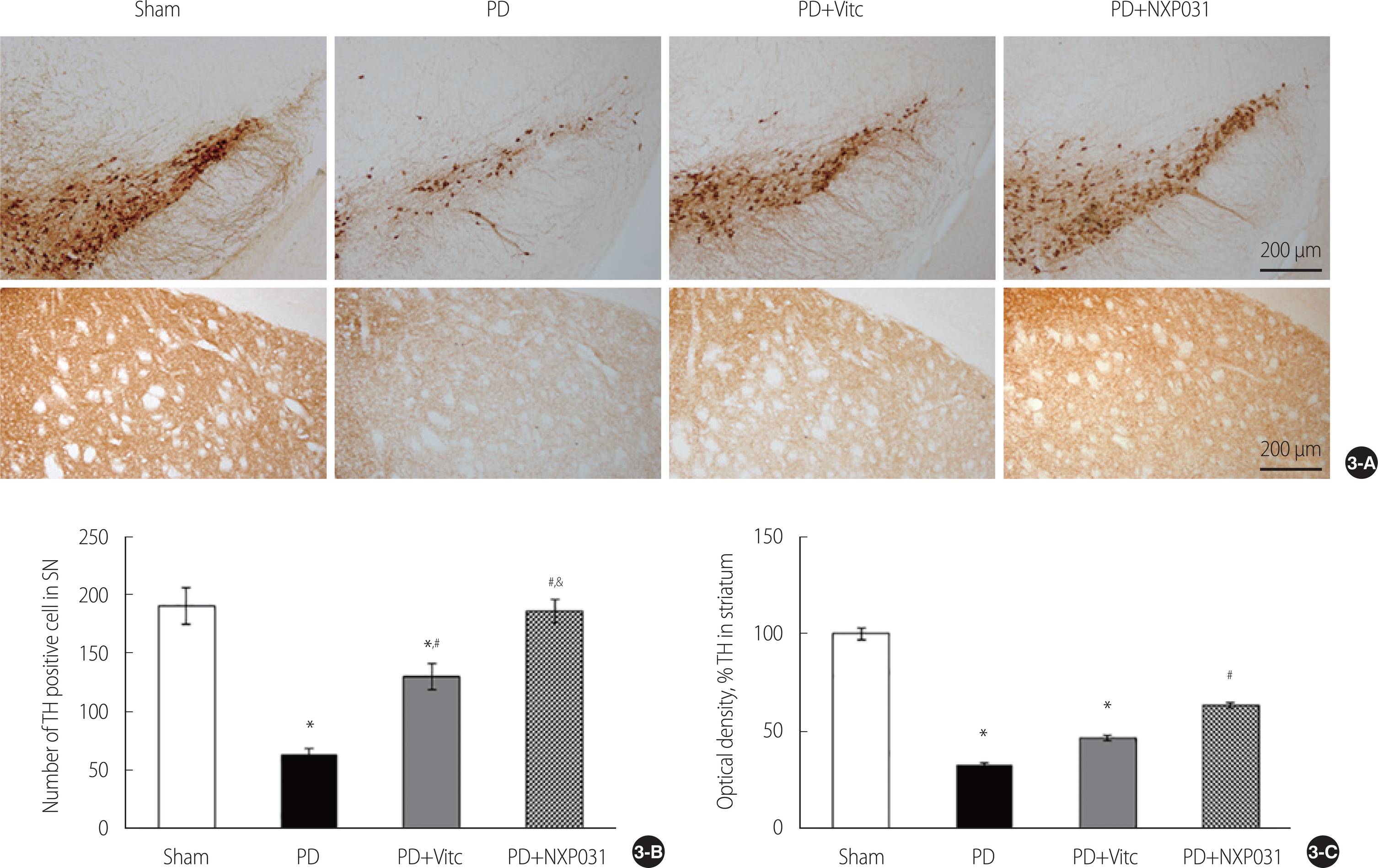
Effect of NXP031 on TH-immunoreactivity. Photomicrographs of TH immunostaining in the SN and striatum (A), the number of TH-positive cell in SN (B), the optical density (%) in the striatum (C). Data are expressed as mean±S.E.M. S.E.M: Standard error of the mean. *Significantly different from Sham, #significantly different from PD, &significantly different from PD+VitC. Scale bar=200 μm. PD=Parkinson’s disease; VitC=Vitamin C.
2) 미세아교세포의 반응성
미세아교세포의 반응성을 확인하기 위해 흑질 부위에 Iba1 항체를 면역조직화학법을 통해 관찰한 결과 Sham 그룹에 비해 PD 그룹에서 미세아교세포의 활성 면적이 3배 이상 증가하는 것을 확인할 수 있었다(p<.001). PD+VitC 그룹은 PD 그룹과 차이가 없어(p=.111) 미세아교세포의 반응성이 개선되지 않았다. 반면에 PD+NXP031 그룹은 PD 그룹에 비해 Iba1으로 염색된 면적이 거의 1/3로 감소되었으며(p<.001) 이러한 형태학적 변화는 vitamin C를 투여 받은 그룹에 비해서도 NXP031을 투여 받은 그룹에서 유의하게 감소되는 것을 확인할 수 있었다(p<.001). 이로써 NXP031의 복강내 투여는 도파민성 신경세포의 손상의 감소뿐만 아니라 미세아교세포의 활성을 감소시키는 것을 확인 할 수 있었다(Figure 4).
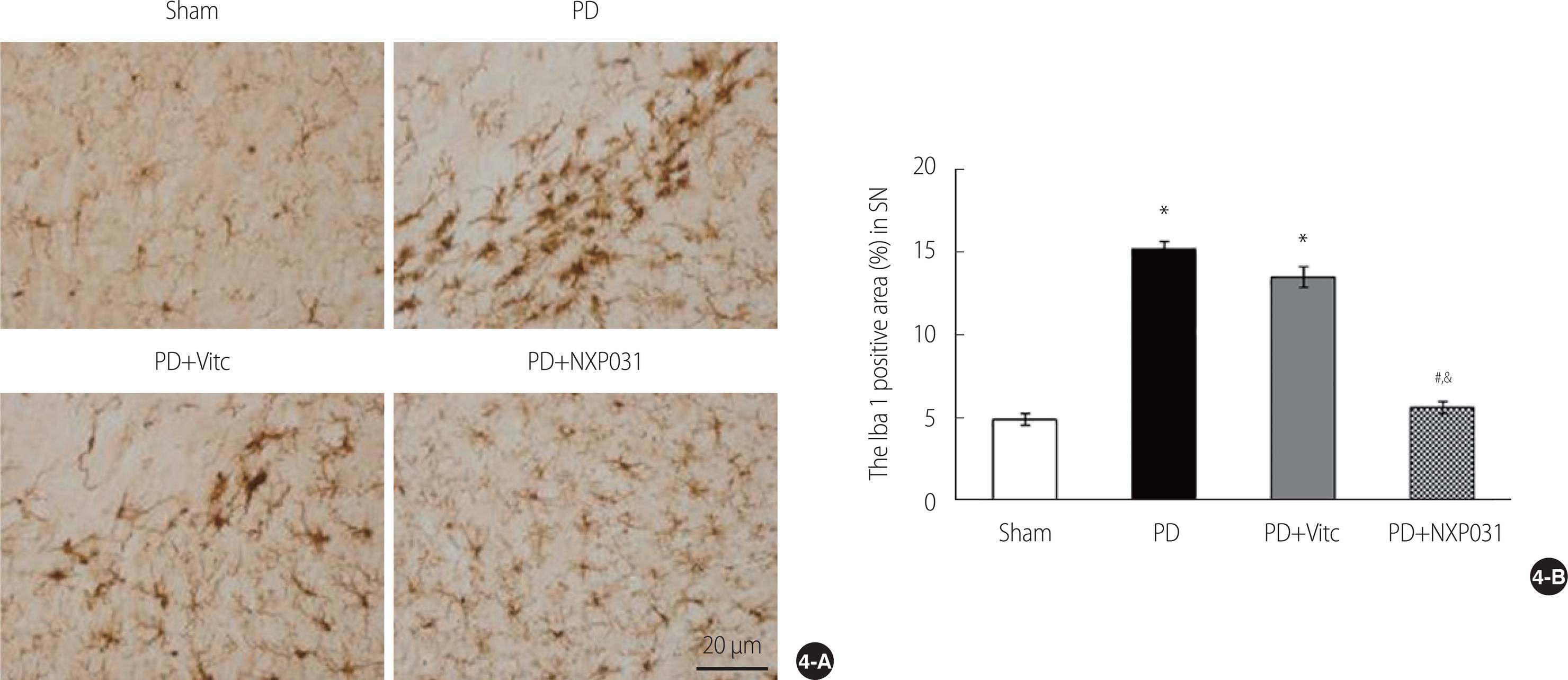
Effect of NXP031 on microglia activity. Photomicrographs of Iba1 immunostaining in the SN (A), the Iba1 positive area (%) in SN (B). Data are expressed as mean±S.E.M. S.E.M: Standard error of the mean. *Significantly different from Sham, #significantly different from PD, &significantly different from PD+VitC. Scale bar=20 μm PD=Parkinson’s disease; VitC=Vitamin C.
논 의
본 연구를 통해 vitamin C의 항산화 효율성을 높인 NXP031이 MPTP로 유도된 아만성 PD 동물 모델의 흑질과 선조체에서 도파민성 신경세포의 손상을 감소시켰으며 PD의 주된 임상 증상인 운동 장애를 억제하는 것을 확인하였다. 또한 행동장애 및 도파민성 신경세포의 병리적 개선과 함께 미세아교세포의 활성이 감소되는 것을 발견하였다.
Vitamin C는 인간 유기체에 필수적이고 뇌발달에 중요하며[34] 콜라겐 생성을 통한 혈관 신생, 산화질소 대사 감소, 그리고 카테콜라민의 합성[35]의 기능을 갖는다. Vitamin C와 PD의 관련 연구로는 인간신경아세포종 세포주(human neuroblastoma cell line)와 AA (100-500 mM)를 2시간 동안 함께 배양한 결과 용량 의존적으로 3,4-dihydroxyphenylalanine (DOPA)과 도파민의 합성이 증가되었고, 도파민 신경세포의 마커로 속도 제한 효소인 tyrosine hydroxylase (TH)유전자의 발현은 3배 증가하였다[36]. 또한 AA를 처치한 E12 rat의 중뇌에서 유래한 CNS 전구체 세포에서 도파민 세포 분화가 10배 증가 되었다고 보고되었다[37]. 또한 최근의 대규모 코호트 보고에 의하면 17.6년의 추적 관찰 결과 vitamin C, E의 섭취는 PD의 발생 위험에 반비례한다는 결과가 발표되었다[38]. 그럼에도 세포 결과나 코호트 연구 결과는 vitamin C의 작용과 PD에 대한 상관관계를 확립하기에는 여전히 불충분하다. 이에 본 연구에서는 MPTP 로 유도된 아만성 PD model에 vitamin C를 효율적으로 전달하기 위해 개발된 물질인 NXP031 [27,39]을 적용하여 그 효과를 확인 하였다.
MPTP로 인해 유발되는 신경 독성은 산화 스트레스, 미토콘드리아 기능부전, α-synuclein의 생성, 그리고 신경 염증 과정을 통해 흑질과 선조체에서 도파민 신경세포의 사멸을 초래하게 된다[40]. 본 연구 결과에서도 MPTP 그룹이 정상군에 비해 흑질과 선조체의 도파민 신경세포(TH+)가 30% 밖에 남아 있지 않아 도파민 신경세포의 사멸을 확인할 수 있었다. NXP031은 vitamin C만을 단독으로 적용한 그룹에 비해 운동기능을 개선시켰으며 뇌의 흑질과 선조체에서 TH+의 손상을 감소시켰다. 급성 독성 모델로 진행된 선행 연구에서는[28] 흑질과 선조체의 TH+ 세포가 거의 동일한 수준으로 회복되었고 본 연구에서도 흑질 부위의 회복은 정상군 수준으로 증가되었으나 선조체는 정상군의 60% 수준으로 회복되어 선행연구와 차이가 있었다. 이는 MPTP의 투여 기간에 따른 MPP+의 용량과 직접적인 상관관계가 있는 것으로 사료되나[41] MPP+를 직접적으로 측정하지 않아 단정할 수는 없다.
Vitamin C는 대뇌 피질, 해마 및 편도체에 풍부하게 존재하며 vitamin C의 환원된 형태인 AA는 수용성으로 혈액-뇌 장벽을 통과할 수 없으나 혈액에서 뇌척수액으로, 뇌척수액에서 신경세포로 sodium-dependent vitamin C transporters 2 (SVCT2)로 능동 수송되며 혈장보다 신경세포에서 100배 이상의 높은 농도로 유지된다[42]. SVCT2 수용체의 발현은 염증과 산화 스트레스에 영향을 받으며 세포 외의 AA의 증가는 신경세포 표면에서 SVCT2의 증가를 유도하여 AA의 세포내 흡수를 증가시키게 된다[43]. 뇌는 산화적 손상에 취약한 기관으로 항산화 효소 및 기전이 매우 중요하나 노화와 함께 일어나는 퇴행성 과정들은 산화적 손상을 피할 수 없다[44]. Vitamin C의 항산화 효능은 매우 탁월하고, 다른 기관에 비해 뇌에 높은 농도로 유지되어 있지만 자체가 친수성이기 때문에 뇌내로의 유입이 쉽지 않으며 뇌에서는 더 큰 항산화 기능이 필요하게 된다[45]. Choi 등[27]은 rGO-SELEX 방식을 이용하여 산화 환원 화학반응에 가장 안정적인 vitamin C와 DNA (aptamer)의 결합 형태를 개발하였고, NXP031(Aptamin C)의 항산화 기능을 ITC analysis를 통해 확인하였다. 또한 이를 적용한 Song 등[28]의 연구에서는 혈장내 AA 농도가 NXP031 그룹에서만 유의하게 높게 유지되어 NXP031이 AA의 활성을 높게 유지시키는 것을 알 수 있다.
미세아교세포는 뇌의 방어 시스템을 대표하는 대식세포로 정의되며 신경염증 반응에 관여하며 파킨슨병 뿐만 아니라 뇌 허혈, 알츠하이머병, 헌팅턴 병과 같은 다양한 신경학적 발병과 강하게 관련된다[46]. 미세아교세포의 활성은 싸이토카인 및 ROS를 과잉 분비하게 하며 혈액-뇌 장벽을 붕괴하여 성상세포 증식을 자극하고 더 많은 미세아교세포를 모이게 하여 결국 신경손상을 일으킨다[47]. NXP031의 복강내 투여는 MPTP로 인한 미세아교세포 활성화를 차단하고 도파민성 신경세포의 소멸을 감소시켜 운동기능의 손상을 완화시키는 것을 확인할 수 있었다. 이러한 결과는 이전의 급성 PD 모델에서 NXP031 투여로 인한 결과와 일치된다[28]. 그러나 아만성 모델에서는 지속적인 MPTP 투여로 인해 운동 협응을 평가하는 rotarod 검사에서 큰 결핍을 보여주었으며 MPP+ 독성에 의해 손상된 운동 기능을 NXP031이 보호하는 것을 파악할 수 있었다. 이러한 결과는 PD의 임상증상인 운동장애를 완화시킬 수 있는 시도라고 사료되며 추후 PD 치료의 병용요법에 사용할 수 있는 잠재적 치료법으로 사용될 수 있을 것이다.
동물모델을 활용한 기초 연구는 사람의 인체에 적용되기 전에 새로운 치료법을 시험하기 위해 사용되며 질병을 더 깊게 이해하는데 도움이 된다. 본 연구는 PD의 생리적 과정에 가깝게 적용하고자 아만성 모델을 시도하여 질병의 특징에 따른 연구를 진행하였다. 이러한 결과는 향후 PD 환자의 정상적인 삶을 위한 치료법 개발에 사용될 수 있을 것이라 사료된다. 더불어 보행기능 및 운동 실조 같은 신경 손상의 회복을 위한 기초간호학적 중재 개발의 기초자료로 활용될 수 있을 것이다. 다만 조직내 도파민 농도와 항산화 능력 정도를 측정하지 못한 것은 제한점이라 할 수 있다.
결 론
NXP031은 MPTP로 유도된 아만성 파킨슨 병 동물 모델에서 손상된 중뇌 흑질과 선조체의 도파민성 신경세포의 결손과 미세아교세포의 활성을 감소시켰다. 또한 파킨슨 병의 대표적인 운동 기능 손상을 개선했다. 이는 NXP031이 만성 퇴행성 질환인 파킨슨병의 예방 및 치료에 활용할 수 있는 신경보호 물질로서의 가능성을 시사한다. 향후 연구에서는 근본적인 도파민성 신경보호 메커니즘을 밝히기 위해 항산화 작용과 혈액-뇌 장벽을 통과하는 과정에 대한 연구가 필요함을 제언하는 바다.
CONFLICT OF INTEREST
The authors declared no conflict of interest.
AUTHORSHIPS
KYJ contributed to the conception and design of this study; LJH and SMK conducted an experiment; LJH and SMK visualized the images; LJH performed the statistical analysis and interpretation; LJH and SMK drafted the manuscript; KYJ and LJH critically revised the manuscript; KYJ supervised the whole study process. All authors read and approved the final manuscript.
ACKNOWLEDGEMENTS
This research is supported by Nexmos (KHU-20182507U0054101 S000100) and National Research Foundation of Korea (NRF) funded by the Ministry of Education, Science and Technology (NRF-2020R1A2B 5B0100276611).